参考资料
P4 高中化学理论主要包括有关物质变化和物质结构的原理,前者涉及化学反应类型如离子反应、氧化还原反应、取代反应、加成反应等)、化学反应与能量变化、化学反应速率、化学平衡,等等;后者包括原子结构、元素周期表和周期律、化学键和分子结构,等等
第一章 物质及其变化 5
第一节 物质的分类及转化 6
同素异形体(allotrope) 树状分类法,交叉分类法 酸性氧化物(acidic oxide),碱性氧化物(basic oxide) 分散系(dispersion system),分散质,分散剂 溶液,乳浊液,悬浊液,胶体(colloid),液溶胶,气溶胶,固溶胶 丁达尔效应 单质到盐的一种转化关系:
graph LR
A[金属单质]--氧气-->B[碱性氧化物]--水-->C[碱]--酸或酸性氧化物-->D[盐]
a[非金属单质]--氧气-->b[酸性氧化物]--水-->c[酸]--碱或碱性氧化物-->d[盐]
第二节 离子反应 14
电解质(electrolyte),熔融状态,电离(ionization),水合离子,电离方程式
酸碱盐的定义
酸:电离时生成的阳离子全部都是氢离子的化合物,叫酸 碱:电离时生成的阴离子全部都是氢氧根离子的化合物,叫碱
盐:酸根离子与金属离子的化合物,叫盐
方法引导:模型
离子反应(ionic reaction),离子方程式(ionic equation) 例如:化学反应 的实质: 强酸与强碱中和反应的实质 Zn 与稀硫酸反应的离子方程式
第三节 氧化还原反应 22
氧化还原反应(oxidation-reduction reaction) 重要特征:反应前后一定存在电子转移(电子得失/共用电子对偏移)有元素的化合价发生变化
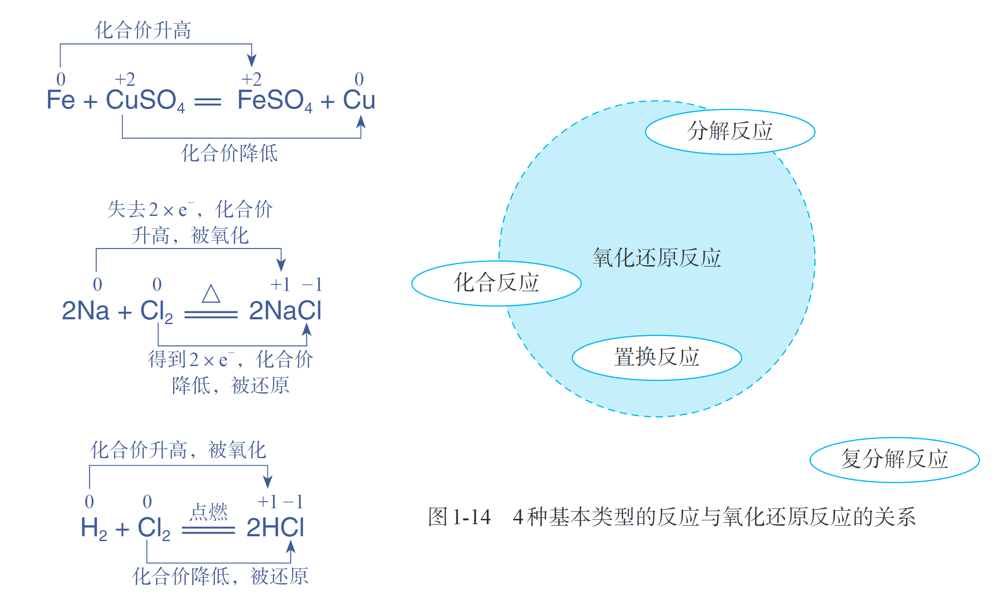
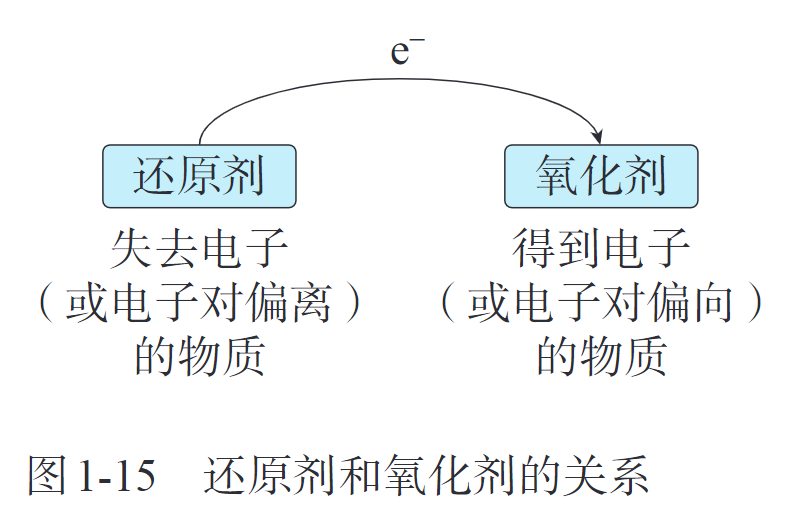
还原剂(reductant),氧化剂(oxidant)
P26 催化转化器
第二章 海水中的重要元素——钠和氯 33
第一节 钠及其化合物 34
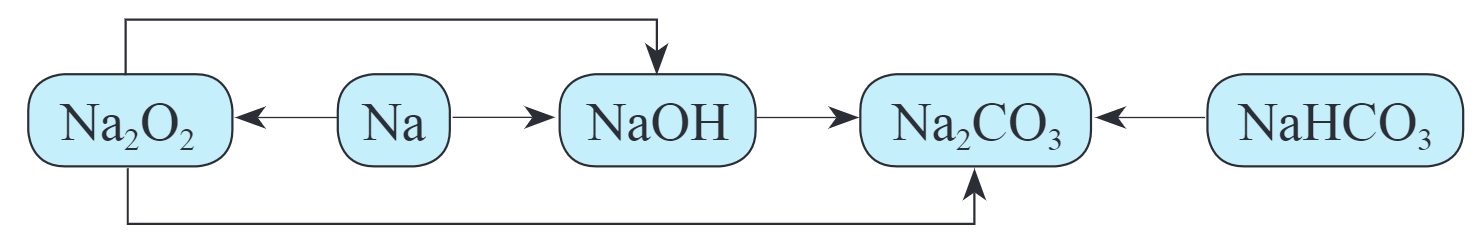
钠(sodium) 钠的几种化合物
- 氧化钠和过氧化钠
- 碳酸钠和碳酸氢钠
碳酸钠晶体——水合碳酸钠()
焰色试验(flame test)

一些金属元素的焰色
| 金属元素 | 锂 | 钠 | 钾 | 铷 | 钙 | 锶 | 钡 | 铜 |
|---|---|---|---|---|---|---|---|---|
| 焰色 | 紫红色 | 黄色 | 紫色 | 紫色 | 砖红色 | 洋红色 | 黄绿色 | 绿色 |
研究与实践:了解纯碱的历史
- 布兰制碱法
- 索尔维制碱法
- 侯氏制碱法
第二节 氯及其化合物 44
氯气(chlorine)
- 与金属、非金属单质的反应
- 与水的反应 次氯酸易分解
- 与碱的反应
氯气的实验室制法
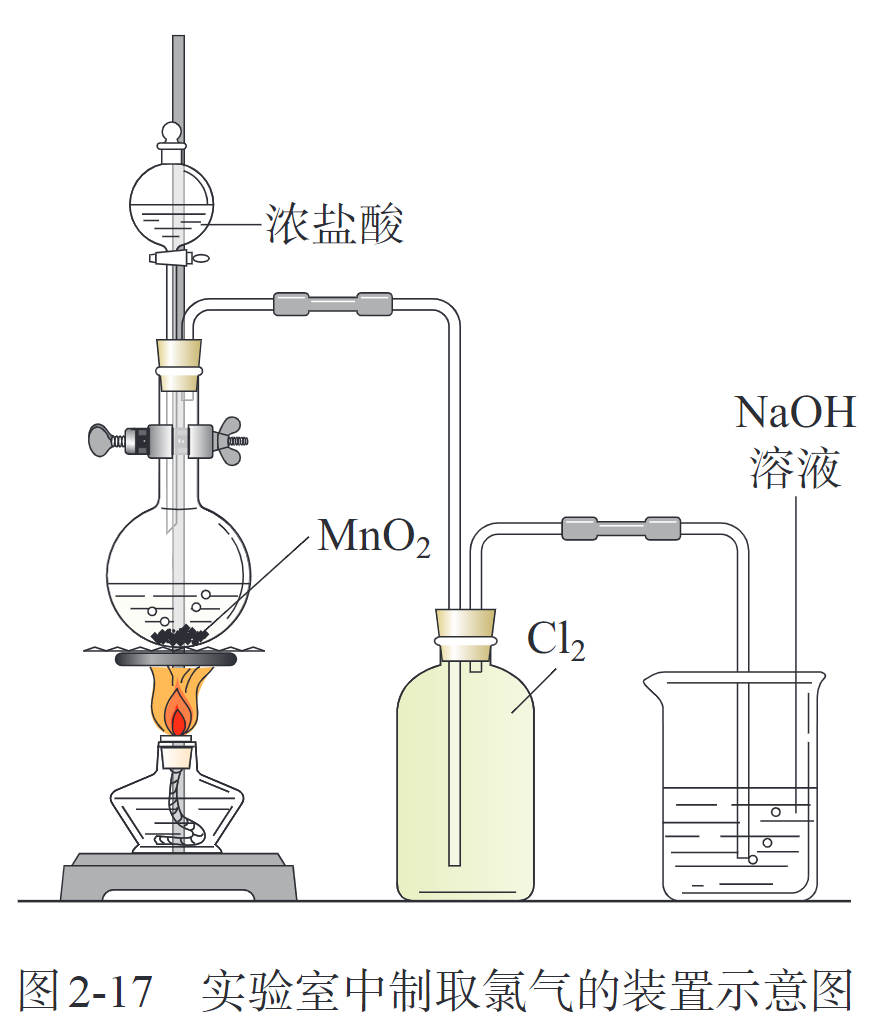 装置的连接顺序一般为:发生装置→除杂装置(如需要)→收集装置→尾气处理装置(如需要)
装置的连接顺序一般为:发生装置→除杂装置(如需要)→收集装置→尾气处理装置(如需要)
氯离子的检验
- 使用稀盐酸 / 溶液
- 使用 溶液 可溶于稀硝酸 可见,检测需要排除干扰
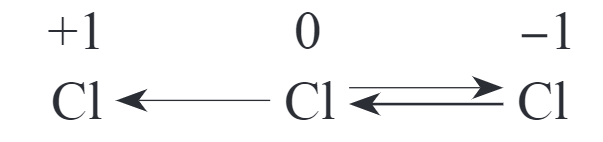
第三节 物质的量 53
物质的量(amount of substance) ,摩尔(mole) 物质的量、阿伏加德罗常数()与粒子数()之间的关系 国际单位制(SI)的 7 个基本单位
| 物理量 | 单位名称 | 单位符号 |
|---|---|---|
| 长度 | 米 | m |
| 质量 | 千克(公斤) | kg |
| 时间 | 秒 | s |
| 电流 | 安[培] | A |
| 热力学温度 | 开[尔文] | K |
| 物质的量 | 摩[尔] | mol |
| 发光强度 | 坎[德拉] | cd |
摩尔质量(molar mass) 物质的量,物质的质量和摩尔质量()之间的关系
气体摩尔体积(molar volume of gas) B 物质的量浓度(amount-of-substance concentration of B) 容量瓶的使用 稀释溶液是常用的计算式
实验活动 1 配制一定物质的量浓度的溶液 65
第三章 铁 金属材料 67
第一节 铁及其化合物 68
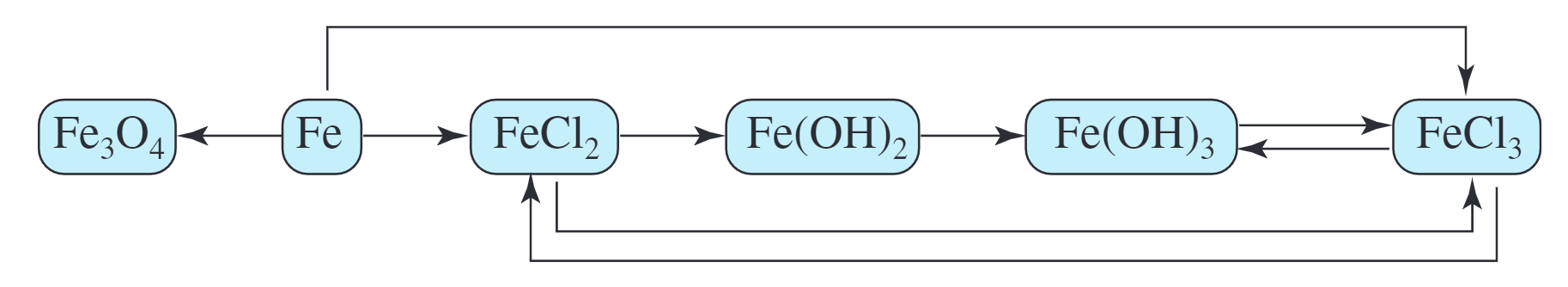
铁(iron) 铁的重要化合物
- 铁的氧化物
- 铁的氢氧化物 氢氧化铁(iron( III ) hydroxide),氢氧化亚铁(iron( II ) hydroxide)
- 铁盐和亚铁盐 P74 利用覆铜板制作印刷电路板
第二节 金属材料 78
合金的优点 铁合金,碳素钢,合金钢(特种钢) 高碳钢,中碳钢,低碳钢
钢中合金元素的主要作用
| 合金元素 | 主要作用 |
|---|---|
| 铬(Cr) | 增强耐磨性和抗氧化性;增强高温强度;提高高碳钢的耐磨性等 |
| 锰(Mn) | 防止硫引起的脆性;增强钢的强度和韧性等 |
| 钼(Mo) | 降低脆性;增强高温强度;提高红热时的硬度和耐磨性等 |
| 钨(W) | 提高高温时的强度和硬度;增强工具钢的耐磨性等 |
| 钴(Co) | 提高红热时的硬度和耐磨性;用于制造磁性合金等 |
| 镍(Ni) | 增强低温时的韧性;改变高铬钢的内部结构等 |
| 硅(Si) | 提高低合金钢的强度和硬度;增强高温时的抗氧化性等 |
铝 四羟基合铝酸钠 铝合金,硬铝
新型合金,储氢合金,钛合金,耐热合金,形状记忆合金
物质的量在化学方程式计算中的应用 化学方程式中各物质的化学计量数之比等于各物质的物质的量之比
实验活动 2 铁及其化合物的性质 90
第四章 物质结构 元素周期律 91
第一节 原子结构与元素周期表 92
元素周期表(periodic table of elements)
原子结构
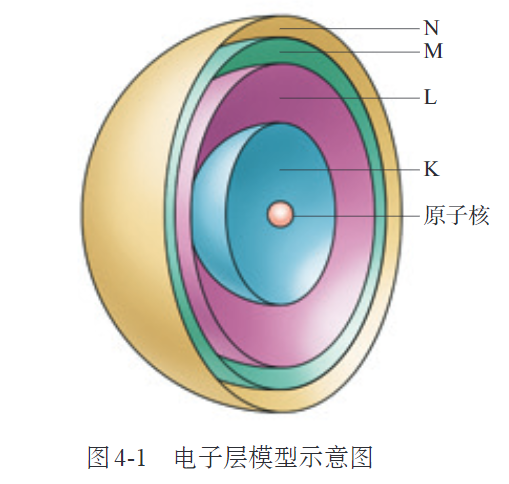
原子序数(atomic number),周期(period),族(group),碱金属元素,卤族元素 核素(nuclide),同位素(isotope)
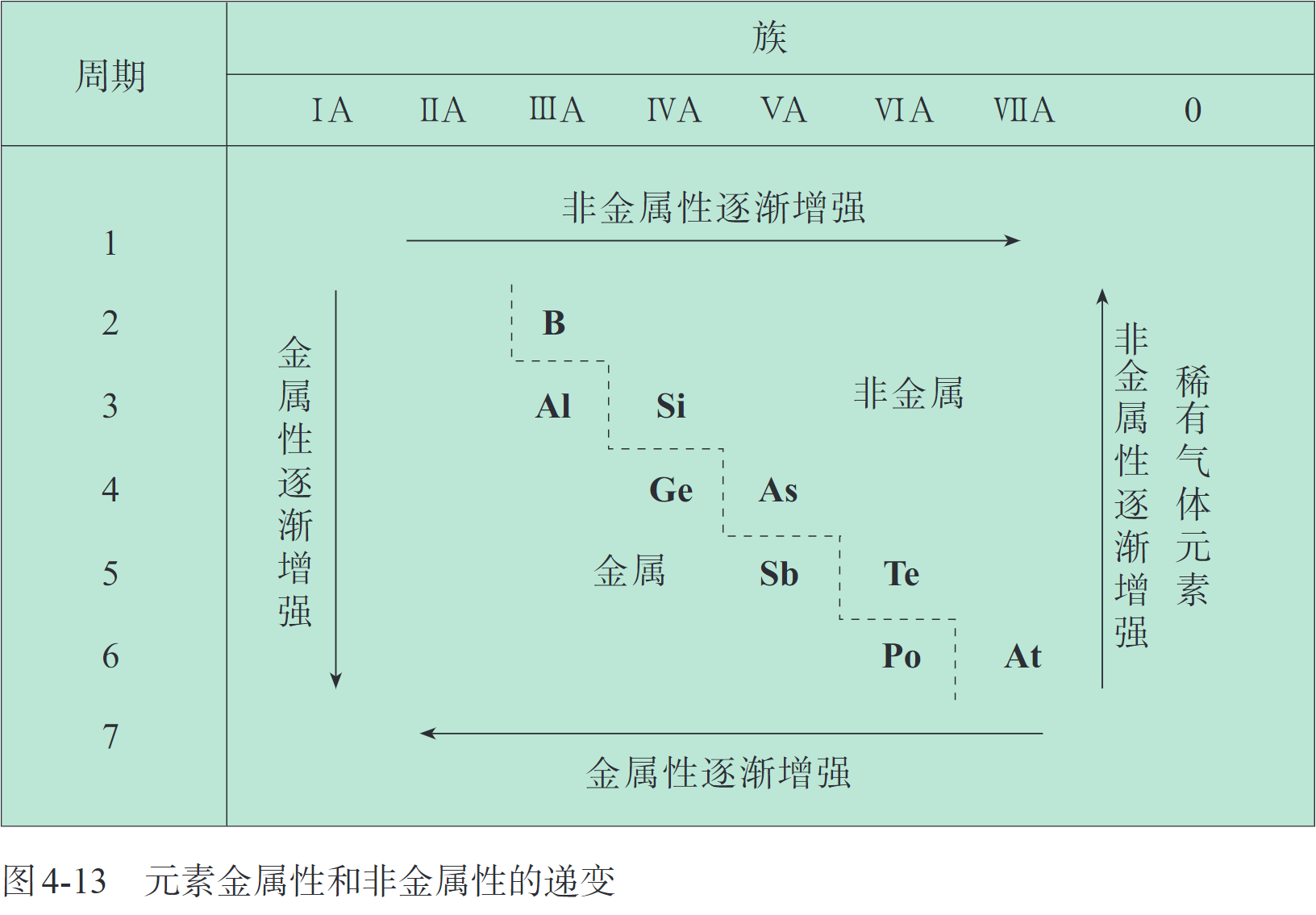
原子结构与元素的性质 金属性,非金属性
- 碱金属元素
- 卤族元素(简称卤素)
P101 方法引导:预测
第二节 元素周期律 107
元素周期律(periodic law of elements)
 元素的化合价与元素在周期表中的位置的关系
元素的化合价与元素在周期表中的位置的关系
第三节 化学键 113
离子键(ionic bond),电子式,结构式,共价键(covalent bond),极性共价键(简称极性键),化学键(chemical bond)
分子间作用力(范德华力),氢键
实验活动 3 同周期、同主族元素性质的递变 122
一些常见元素中英文名称对照表 128
| 元素符号 | 中文 | 英文 | 元素符号 | 中文 | 英文 |
|---|---|---|---|---|---|
| Ag | 银(yín) | silver | Al | 铝(lǚ) | aluminum |
| Ar | 氩(yà) | argon | Au | 金(jīn) | gold |
| B | 硼(péng) | boron | Ba | 钡(bèi) | barium |
| Be | 铍(pí) | beryllium | Br | 溴(xiù) | bromine |
| C | 碳(tàn) | carbon | Ca | 钙(gài) | calcium |
| Cl | 氯(lǜ) | chlorine | Co | 钴(gǔ) | cobalt |
| Cr | 铬(gè) | chromium | Cu | 铜(tóng) | copper |
| F | 氟(fú) | fluorine | Fe | 铁(tiě) | iron |
| Ga | 镓(jiā) | gallium | Ge | 锗(zhě) | germanium |
| H | 氢(qīng) | hydrogen | He | 氦(hài) | helium |
| Hg | 汞(gǒng) | mercury | I | 碘(diǎn) | iodine |
| K | 钾(jiǎ) | potassium | Kr | 氪(kè) | krypton |
| Li | 锂(lǐ) | lithium | Mg | 镁(měi) | magnesium |
| Mn | 锰(měng) | manganese | N | 氮(dàn) | nitrogen |
| Na | 钠(nà) | sodium | Ne | 氖(nǎi) | neon |
| Ni | 镍(niè) | nickel | O | 氧(yǎng) | oxygen |
| P | 磷(lín) | phosphorus | Pb | 铅(qiān) | lead |
| Pt | 铂(bó) | platinum | Ra | 镭(léi) | radium |
| Rn | 氡(dōng) | radon | S | 硫(liú) | sulphur |
| Sc | 钪(kàng) | scandium | Se | 硒(xī) | selenium |
| Si | 硅(guī) | silicon | Sn | 锡(xī) | tin |
| Sr | 锶(sī) | strontium | Ti | 钛(tài) | titanium |
| U | 铀(yóu) | uranium | V | 钒(fán) | vanadium |
| W | 钨(wū) | tungsten | Xe | 氙(xiān) | xenon |
| Zn | 锌(xīn) | zinc |